近日,迪必尔生物结束了第15届国际代谢工程大会(Metabolic Engineering 15)的行程。生物工艺工程师赵北辰先生在大会现场以海报的形式展示了研究成果《An Open-Source Digital Twin Framework for Intelligent Biomanufacturing》。
该研究对生物过程数字孪生的概念进行了界定,提出了开源的生物过程数字孪生框架,并且针对细胞培养进行了案例研究,体现了数字孪生在过程分析技术(PAT)和高级过程控制(APC)领域的巨大潜力。本文将对该研究的具体内容和技术细节进行解读。

该研究在迪必尔生物李雪良博士、江南大学李江华教授和关欣副研究员的指导下完成,相关学术论文发表《Processes》。(https://doi.org/10.3390/pr11041213)
基于数字孪生的生物制造系统是以数字孪生为核心,软硬件多层次、多尺度深度结合的动态系统,从数据流的角度来看(图1),该系统以集成在制造系统上的在线传感器为数据来源,通过统一的数据接口传输至数字孪生,经过数据同步、处理和预测后,用于系统自我修正的高阶数据从数字孪生和物理实体间的双向数据通道返回,关键数据经可视化后展示在HMI上,而操作人员的指令则通过HMI传输回数字孪生和物理实体。
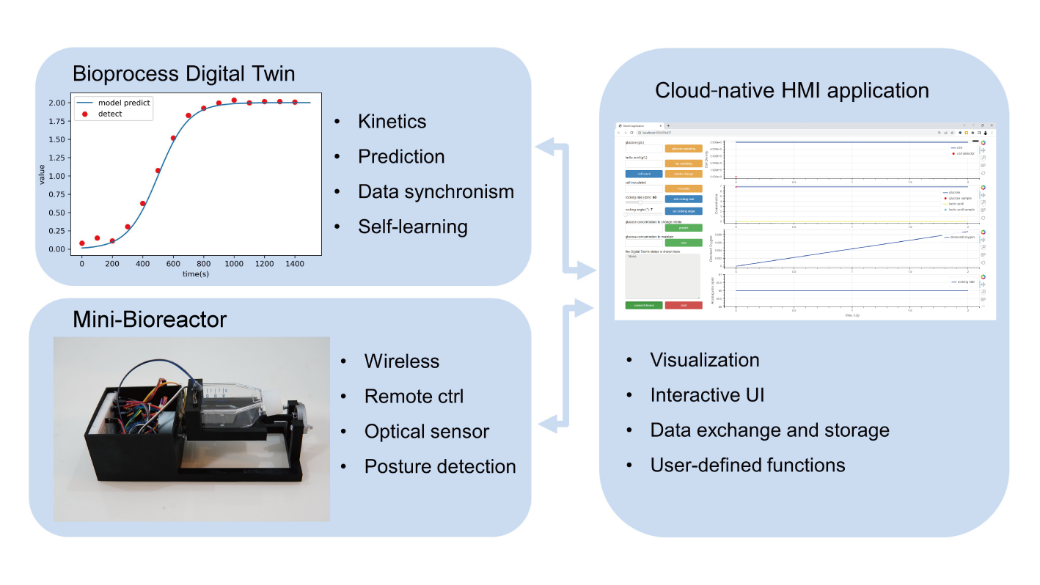
图1 基于数字孪生的细胞培养系统架构设计
基于上述思路,该研究基于Python与C++混合编程技术,开发了基于数字孪生的开源细胞培养框架,包含数字孪生、微型反应器(支持在线细胞密度检测)和web端HMI应用。其中数字孪生与微型反应器分别连接至HMI,进行交互与数据管理。该框架已开源,欢迎下载体验。(https://github.com/BeichenZhao/BioDT)
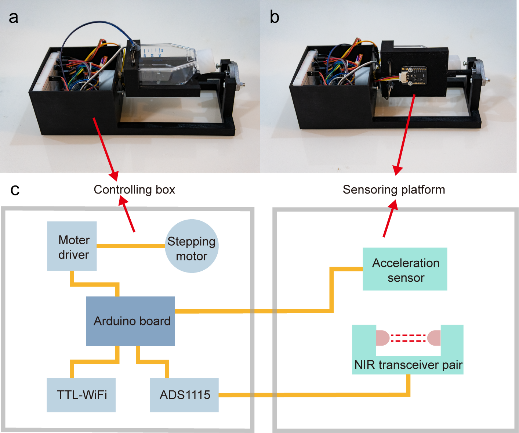
数字孪生在过程分析技术(PAT)和高级过程控制(APC)方面的潜力引人注目。然而,在生物制造领域,尚未出现成熟的基于数字孪生的制造执行系统(MES)。数字孪生究竟可以给人们带来什么样的帮助呢?该研究通过两个案例研究,对这一问题进行初步阐述:
基于上述基于数字孪生的细胞培养系统,针对中国仓鼠卵巢细胞进行实验。首先开发了基于数字孪生的预测结果进行手动换液提醒功能。换液是在细胞培养中的常规操作,其目的是弃掉旧的培养基,换成新鲜的培养基来为细胞提供营养支持。那么,在什么时间点换液,既能维持细胞的生长代谢,又不造成培养基的浪费,成了研究人员关注的问题。
本研究基于代谢物浓度,在HMI上集成了一个提示功能,如图3所示,以葡萄糖为例,通过点击“predict”按钮,就可以得到未来一段时间内,葡萄糖和细胞密度变化的预测结果。

为了验证预测结果的准确性,分别以葡萄糖和乳酸浓度为检测指标开展了实验,在不同的初始细胞接种密度下,预测值分别达到4 g/L和1 g/L时,进行换液并离线取样测试。离线取样的数据一方面是为了验证预测结果的准确性,另一方面是为了通过HMI将该数据同步至数字孪生,校准其预测结果,更新其动力学参数。结果表明,该数字孪生系统可以准确地预测代谢物浓度,为研究人员的理性决策提供参考。同时也能看出,预测结果的偏差总体呈现出随时间缩小的趋势,这受益于数字孪生对动力学参数的更新,从而使数字孪生可以更精准地追踪系统的状态。

图4 (a-c)在2, 5和10 (×106) cell·mL-1的初始接种密度下以葡萄糖浓度为指标进行手动换液提醒;(d-f)在2, 5和10 (×106) cell·mL-1的初始接种密度下以乳酸浓度为指标进行手动换液提醒
然而,换液仍然需要研究人员手动操作,为了探究数字孪生系统的自动化能力研究人员在控制系统中集成了一个蠕动泵,以实现对葡萄糖浓度的调节。如图5所示。数字孪生模型根据机理模型和历史数据实时预测培养基中的葡萄糖浓度。当预测的葡萄糖浓度低于5 g/L时,蠕动泵自动开启,执行一次补料动作。用控制论的术语来说,这实现了对葡萄糖的模型预测控制(Model Predicting Control, MPC)。
如图6所示,为了验证模型预测的准确度和控制效果的稳定性,每隔12h进行一次葡萄糖离线取样测量,结果表明,基于数字孪生的模型预测控制可以将葡萄糖浓度稳定地维持在5g/L。此外,与批次培养相比,在48 h的培养后,该策略使细胞得率提高了14.8%。
图6(a)进行葡萄糖补料的葡萄糖浓度变化;(b)是否使用葡萄糖自动补料的细胞密度比较
那么,数字孪生是如何被构建出来的呢。以本研究为例,细胞培养中的各项参数主要通过各种动力学方程计算,下面列举主要计算公式。
细胞密度使用Logistic方程计算:
其中,μ代表特定生长速率 (cell/cell);μmax代表最大生长速率 (cell/cell);X代表细胞密度 (cell/mL);Xmax代表最大细胞密度 (cell/mL)。
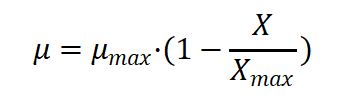
底物代谢用以下公式计算:
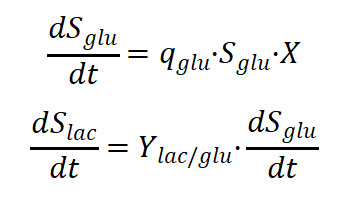
其中Sglu是葡萄糖浓度(g/L); Slac是乳酸浓度 (g/L); qglu是葡萄糖代谢速率 (L/g/cell/h);Ylac/glu是乳酸产率 (g/g).
此外,每当传感器数据或离线检测数据同步至数字孪生,其内置的Levenberg-Marquardt算法就会对动力学参数进行重新测算,使其更好的捕捉细胞当前的生理状态。
数字孪生具备全时空尺度过程重建的能力,由于微型反应器中的流场可以被认为是全混流,在空间上分布基本均匀,该研究把目光放在了全时间尺度,即历史过程重建、当前动力学参数计算和未来状态预测,并在批次培养实验中进行了验证。
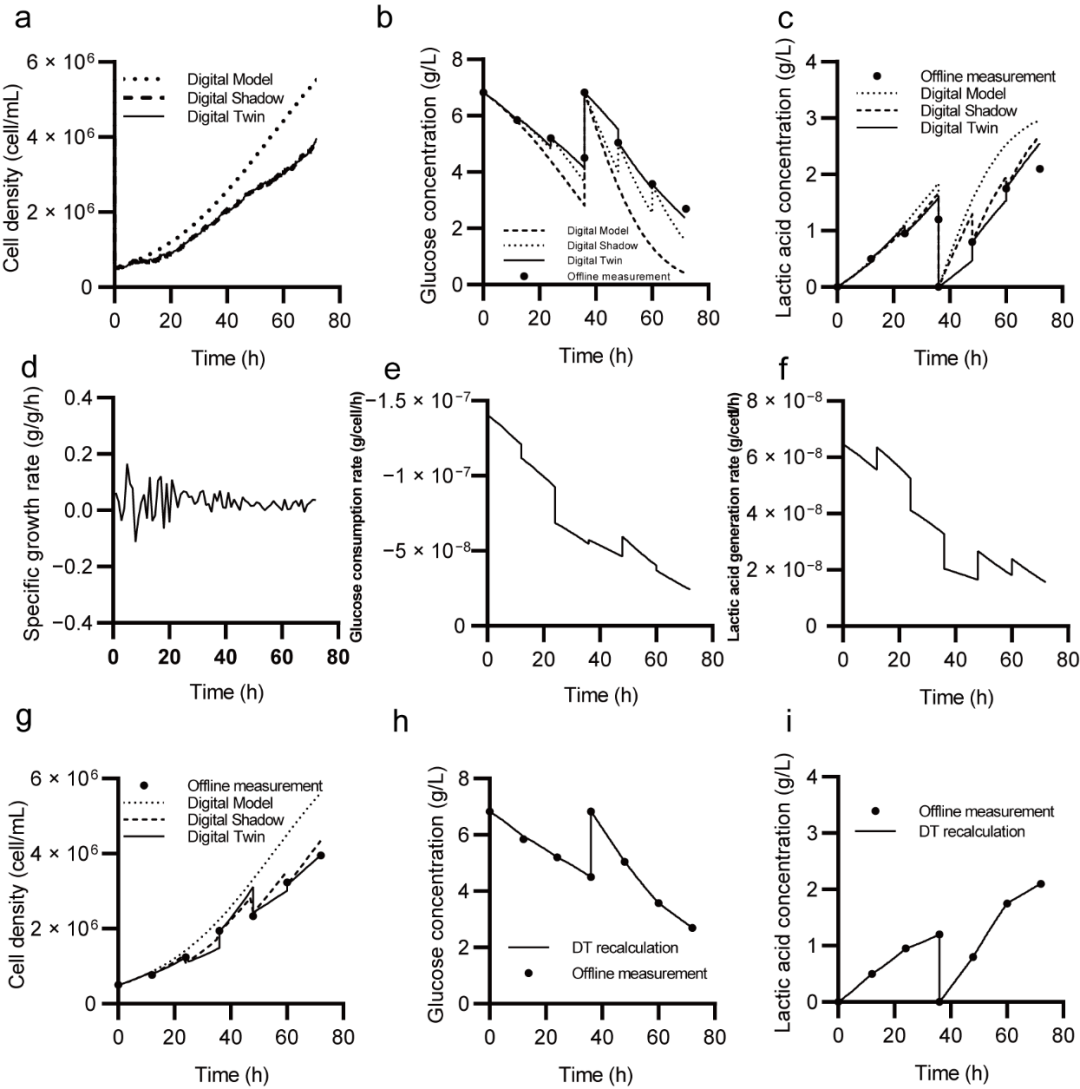
图7 (a)根据传感器数据更新的数字模型、数字映射和数字孪生预测的细胞密度变化值;(b)数字模型、数字映射和数字孪生对葡萄糖消耗的预测;(c)数字模型、数字映射和数字孪生对乳酸产生的预测;(d)数字孪生计算的比生长速率;(e)数字孪生计算的葡萄糖消耗速率;(f)数字孪生计算的乳酸产生速率;(g)根据离线测量数据更新的数字模型、数字映射和数字孪生预测的细胞密度变化值;(h)数字孪生重建的葡萄糖浓度变化过程;(i)数字孪生重建的乳酸浓度变化过程
在这里,数字模型(Digital Model)、数字映射(Digital Shadow)和数字孪生(Digital Twin)分别被用于对培养过程中细胞密度的变化进行预测。如图7(a)所示,数字模型的静态预测在开始时与实验数据偏差较小,但随着时间的推移增大。这是因为静态动力学参数无法捕捉细胞生理代谢的变化,导致累积误差无法消除。数字映射和数字孪生每15分钟与传感器数据同步一次,获得了更准确的追踪结果。此外,数字孪生还提供了比生长速率的变化情况(图7(d)),由于一旦传感器数据传回,该值就会更新。仅用于跟踪过程参数而言,在高采样频率下,数字孪生相对于数字映射的优势并不明显。
如果只有离线测量数据可用,由于更新周期较长,即使数字映射周期性地进行了校正,误差也会随着时间的推移扩大(图7(g))。数字孪生基于传感器数据更新了μmax,从而跟踪了细胞生理活性和比生长速率的变化(图7(d)),获得了更加准确的预测结果。
葡萄糖消耗和乳酸生成也分别通过数字模型、数字映射和数字孪生进行了预测,如图7(b)(c)所示。基于获取的数据,经动力学参数校正的数字孪生成功捕捉到了葡萄糖和乳酸浓度的变化,相较于数字模型和数字映射,预测结果更加准确。利用数字孪生,还计算出了葡萄糖消耗速率和乳酸生成速率,显示出随时间的总体下降趋势(图7(e)(f))。这种现象可能是由于葡萄糖浓度降低和细胞密度增加而导致的代谢活性减少。这些实验结果表明了数字孪生在追踪细胞代谢方面的能力,这对于理解处在动态变化环境下的细胞活性变化至关重要。
图7(h)(i)展示了通过利用数字孪生获得的更新参数重新计算历史的细胞密度、葡萄糖浓度和乳酸浓度的过程趋势。由于离线数据仅反映了时间上离散的培养过程。通过重建整个培养过程,数字孪生使研究人员能够更全面地研究历史过程的条件,从而获得对所研究的生物系统更详细和准确的理解。
随着数字孪生在各行各业的发展,人们逐步意识到这是一个极具发展潜力的概念,很有可能会变革未来的生物制造模式。在物联网的概念流行的时代,我们常说“万物互联”,现在我们已经能无感地享受到传感器的普及给我们带来的便利。TJX团队认为,我们有机会迎来一个“万物皆可计算”的时代,从基因表达、酶促反应,到细胞生长代谢,再到反应器流场仿真,从而建立代谢模型与计算流体力学耦合的多尺度、多层次模型,并且在工艺开发的各个阶段为工艺开发人员提供建议。或许在不久的将来,上位机软件的数据展示界面中出现各个参数的预测曲线,会成为一件稀松平常的事情。